Fieberhaft
Wie ein Experte der Freien Universität und des Max-Planck-Instituts für Kolloid- und Grenzflächenforschung mit der Synthese von Kohlenhydraten gegen Malaria kämpft
01.07.2013
Eigentlich war es für Professor Peter Seeberger „nur“ Grundlagenforschung zur Synthese von Kohlenhydrate, geworden ist es aber ein Spezialgebiet für Malaria-Impfstoffe.
Bildquelle: istockphoto/LanceB
Wer sich als Wissenschaftler für die Grundlagenforschung entscheidet, weiß selten vorher, wohin die Reise geht. Peter Seeberger, Professor an der Freien Universität Berlin und Direktor am Max-Planck-Institut für Kolloid-und Grenzflächenforschung in Potsdam, interessiert sich in erster Linie für die Synthese von Kohlenhydraten. Dass ihn dieses Spezialgebiet einmal zu einem Experten in Sachen Malaria-Impfstoffe machen würde, konnte er nicht ahnen. Und dass ein quasi nebenbei entwickeltes photochemisches Syntheseverfahren, das mit Kohlenhydraten gar nichts zu tun hat, die Kosten für die Herstellung eines der wichtigsten Malariamedikamente mehr als halbieren würde, war auch nicht abzusehen.
Es gibt dieses eine Foto von ihm, das eigentlich schon alles sagt. In einer Broschüre zum Körber-Preis für die Europäische Wissenschaft, mit dem Peter Seeberger im Jahr 2007 ausgezeichnet wurde, ist es abgedruckt. Der Wissenschaftler rennt in Anzughose und Hemd über eine quietschgrüne Wiese. Die Kamera wurde mitgezogen, der Hintergrund ist verwischt. Immer unterwegs, sagt das Bild. Zum nächsten Termin. Zur nächsten Entdeckung.
Zeit ist eine knappe Ressource. Während Peter Seeberger in seinem geräumigen Büro an der Freien Universität über die Malaria-Forschung spricht, tickt die Uhr. Bill Gates ist in Berlin. Der Multimilliardär trifft Peer Steinbrück, Dirk Niebel und – Peter Seeberger. Gesprochen werden soll über die Malaria-Forschung, genauer über ein neuartiges Syntheseverfahren für das Malaria- Medikament Artemisinin. Der Wirkstoff mit den drei „i“ im Namen hat in den letzten Jahren in der Welt der Pharmakologie eine Karriere hingelegt, die ihm noch bis vor Kurzem kaum jemand zugetraut hätte. Peter Seeberger und seine Kollegen schicken sich gerade an, ein spannendes neues Kapitel dazu beizutragen.
Siegeszug einer Heilpflanze
Aber der Reihe nach: Artemisinin ist einer von ein paar hundert Inhaltsstoffen des einjährigen Beifuß, einer Heilpflanze, die unter dem Namen Qinghao seit Jahrhunderten in Ostasien angebaut und im Rahmen der traditionellen chinesischen Medizin als Fiebersenker eingesetzt wird.
Schon in den 1970er Jahren wurde Artemisinin von der chinesischen Pharmakologie-Professorin Tu Youyou chemisch beschrieben und seither in Ostasien gegen Malaria eingesetzt. Erst nach dem Ende des Kalten Krieges begannen sich auch westliche Mediziner und die Weltgesundheitsorganisation WHO für das pflanzliche Heilmittel zu interessieren. Seit einigenJahren empfiehlt die WHO Artemisinin in vielen Teilen der Welt als wesentlichen Bestandteil der Malaria-Therapie, vor allem deswegen, weil es nicht nur hoch wirksam, sondern auch vergleichsweise gut verträglich ist. Es gibt allerdings ein Problem. Artemisinin ist teuer. Es muss aus der an sich günstig anzubauenden Beifuß- Pflanze aufwendig extrahiert werden. „Der einjährige Beifuß enthält etwa 0,4 bis 1,2 Prozent Artemisinin. Die derzeit eingesetzten Extraktionsverfahren führen zu einem Preis von bis zu 1200 Dollar pro Kilogramm“, sagt Seeberger. Der Versuch, Artemisinin gentechnisch zu erzeugen, um sich die Extraktion zu sparen, war bisher nur begrenzt erfolgreich. Was also tun?
Der Artemisinin-Synthese geht ein Licht auf
Dass Seeberger überhaupt mit Artemisinin in Berührung kam, verdankte sich einem Zufall: „Ich hatte von dieser Substanz bis vor ein paar Jahren noch nie etwas gehört.“ Der Forscher ist eine Koryphäe auf dem Gebiet der automatisierten Kohlenhydratsynthese.
Aber auch andere chemische Synthesen beschäftigen ihn: „Wir haben eine Zeit lang mit Photochemie gearbeitet, um Nanopartikel definierter Größe zu erzeugen, die beispielsweise für die Herstellung von Kunststoffscheiben oder Kompaktkleber verwendet werden können.“ Bei photochemischen Synthesen werden die Ausgangssubstanzen allein durch Einwirkung von Licht in das gewünschte Endprodukt überführt. In der Pharmaindustrie wird dieses Verfahren bisher allerdings kaum verwendet, weil das Licht nicht tief genug in die großen Tanks der industriellen Wirkstoffsynthese eindringt.
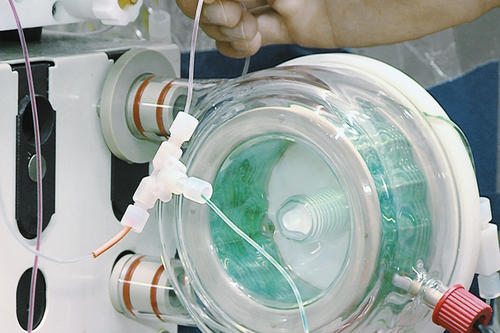
Seeberger und seine Kollegen kamen nun auf die Idee, für die photochemische Synthese ein Durchflussverfahren zu entwickeln. „Unser Ziel war letztlich, eine praktikable Synthesemethode fürs Labor zu entwickeln, mit der wir größere Mengen unterschiedlicher Wirkstoffe erzeugen können“, sagt Seeberger. Gedacht, getan: Ein lichtdurchlässiger Schlauch wurde um eine Lichtquelle gewickelt. Dadurch konnte die durch den Schlauch fließende Ausgangssubstanz, damals war das Sauerstoff, dem Licht sehr gleichmäßig und vor allem gut kontrollierbar ausgesetzt werden. Es entstand hochreaktiver Singulett-Sauerstoff für zahlreiche chemische Reaktionen. Am Ende tropfte das gewünschte Endprodukt aus dem Schlauch.
„Wir fanden das spannend, weil wir den Eindruck hatten, dass sich mit dieser relativ einfachen Methode vieleschöne Reaktionen in großem Maßstab auslösen ließen“, erinnert sich Seeberger. Als er über seine photochemische Durchflusssynthese vor zwei Jahren auf einer Konferenz referierte, kam nach dem Vortrag ein Zuhörer nach vorn. Er berichtete von einem Malaria-Medikament namens Artemisinin, das eine Peroxidstruktur aufweise, die extrem schwer zu synthetisieren sei. Ob er da helfen könne? „Wir konnten“, sagt Seeberger.
Wenn Artemisinin künstlich entsteht, dann kommt es zu einer farbenfrohen Reaktion: Aus der violetten Artemisininsäure entsteht grünes Artemisinin.
Bildquelle: Ulrich Kleiner
Durchfluss-Synthese ist effizient und kostengünstig
Ein bisschen chemische Tüftelei war natürlich nötig, um die Reaktion zum Laufen zu bringen. Als Ausgangsmaterial dient Dehydroartemisininsäure, kurz DHAA, die sich aus der Beifuß-Pflanze deutlich einfacher gewinnen lässt als der Wirkstoff Artemisinin selbst. Auch synthetisch kann DHAA relativ problemlos hergestellt werden. Hinzugegeben wird ein Photo-Aktivator. Das Gemisch aus Photo-Aktivator und DHAA wird im lichtdurchlässigen Schlauch langsam um die Lichtquelle gepumpt. Sauerstoff kommt von der anderen Seite. Unter dem Einfluss des Photoaktivators reagiert der Sauerstoff mit DHAA. Es folgt eine Kaskade weiterer Reaktionen. Am Ende steht Artemisinin. „Formal handelt es sich um eine Dreistufensynthese“, erläutert Seeberger. Als wir das Verfahren vor einem Jahr zum ersten Mal öffentlich vorgestellt haben, konnten wir 40 Prozent der Artemisininsäure in Artemisinin umwandeln. Mittlerweile sind wir bei 65 Prozent.“
Was sich trocken anhört, könnte weitreichende Konsequenzen für die Malaria-Therapie haben. „Die einfachste Version unseres Synthesereaktors hat die Größe eines Schuhkartons und produziert 150 Gramm Artemisinin am Tag“, sagt Seeberger. Derzeit wird in dem eigens dafür gegründeten Unternehmen ArtemiFlow ein Reaktor entwickelt, der pro Tag 35 Kilogramm Artemisinin produzieren kann. Der weltweite Bedarf liegt bei rund dreihundert Tonnen pro Jahr. Nach der Entwicklungsphase könnten die Produktionskosten für den Reaktor bei 50.000 Euro liegen. Peter Seeberger ist überzeugt, dass damit ein Kilogramm Artemisinin für unter 300 Dollar denkbar werde: „Damit könnte Artemisinin im Prinzip dezentral produziert werden, dort, wo der einjährige Beifuß angebaut wird und die Medikamente benötigt werden.“
Wie genau die neue Synthesemethode Eingang in die Arzneimittelproduktion finden wird, dürfte sich in dennächsten Jahren zeigen. „Wir reden derzeit sowohl mit philanthropischen als auch mit kommerziellen Partnern“, sagt Seeberger. Für denkbar hält er auch ein „gemischtes“ System, bei dem Artemisinin in bedürftigen Ländern im Rahmen philanthropischer Projekte günstig hergestellt, ansonsten aber konventionell von Pharmaunternehmen vertrieben wird. „Das ist dann natürlich nicht mehr unsere Aufgabe, und deswegen gehen wir bei diesem und auch bei einigen anderen Projekten den Weg über die Gründung von Unternehmen“, betont Seeberger. „Wir sind Grundlagenforscher, und ich versuche, meinen Studierenden auch zu vermitteln, dass sie nicht immer sofort an mögliche Anwendungen denken sollen. Andererseits wehre ich mich aber auch gegen die Haltung, wonach Grundlagenforscher einfach nur wissenschaftliche Artikel publizieren. Ich meine, dass es schon erlaubt sein sollte, weiterzudenken. Und ehrlicherweise muss ich zugeben, dass die Folgeschritte mitunter schwieriger sind als der akademische Teil.“
Kohlenhydratimpfstoff gegen die Malaria?
Dass das so ist, hat Seeberger bei einem medizinisch verwandten, chemisch aber doch ganz anderen Thema schon einmal erfahren: Zusammen mit seinem Team hat er vor einigen Jahren ein Kandidatenmolekül für einen Malaria-Impfstoff entwickelt. An sich ist dieser Impfstoff sehr viel näher an Seebergers eigentlicher Leidenschaft, der Kohlenhydratbiochemie, als Artemisinin. Auf diesem Gebiet hat er vor vielen Jahren am Massachusetts Institute of Technology die Grundlagen für eine automatische Synthese entwickelt. Und für diese Arbeiten hat er später unter anderem den europäischen Körber-Preis erhalten.
Bei Forschungsarbeiten zur Zuckersynthese kam er mit einem australischen Kollegen in Kontakt, der sich mit Zuckermolekülen an der Zelloberfläche von Plasmodien beschäftigte – den Erregern der Malaria. Damals gelang es, eine ganze Reihe dieser Glykolipide zu synthetisieren. Eines davon hat sich im Tiermodell als hoch wirksamer Impfstoff erwiesen. Die Wissenschaftler berichteten darüber in einer Publikation im Fachmagazin „Nature“, die viel Aufmerksamkeit hervorrief. Als es dann jedoch mit externen Partnern an die Arzneimittelentwicklung ging, geriet die Sache ins Stocken. Unnötigerweise, wie Seeberger findet: „Wir sind immer noch begeistert von diesem Molekül. Es beschäftigt uns bis heute, und wir sind überzeugt davon, dass es bei der Malaria-Impfung eine Rolle spielen wird.“
Glykanforschung bei der Aufholjagd
Insgesamt sei die Synthese von Zuckern deutlich schwieriger als die Synthese der meisten anderen biochemischen Moleküle, betont der Experte. Anders als Peptide bilden Zucker oder „Glykane“ nämlich keine linearen Ketten, sondern stark verzweigte Strukturen. Fünf Mitarbeiter Seebergers haben sich beispielsweise 14 Jahre lang mit der automatisierten Synthese des gerinnungshemmenden Medikaments Heparin herumgeschlagen, bis es endlich gelang: „Das war das härteste Projekt, das wir je hatten“, sagt Seeberger.
Weil Kohlenhydrate so komplex sind, können bisher nur solche Zucker synthetisiert werden, die zehn bis zwanzig Einheiten lang sind. Doch das ändert sich gerade: Seebergers ganzer Stolz ist eine brandneue Synthese-Maschine, die in seinem Labor an der Freien Universität aufgestellt wurde und die es künftig erlauben soll, auch längerkettige Zuckermoleküle synthetisch herzustellen. „Das wird dazu führen, dass sich in Zukunft mehr Wissenschaftler für dieses Feld interessieren“, meint der Experte. „Verglichen mit der Peptidforschung sind wir im Moment noch dreißig Jahre hinterher. Aber die Glykanforschung explodiert gerade.“ Nicht zuletzt die Medizin verspricht spannende Anwendungsfelder: Ob Tumorentstehung, Knorpelwachstum oder Zellstoffwechsel: An all diesen medizinisch hoch relevanten Prozessen sind unter anderem Glykane beteiligt.
Das sind gute Aussichten für die zahlreichen Nachwuchswissenschaftler in Seebergers Abteilung. 75 Mitarbeiter hat er derzeit. Zwei Drittel davon kommen nicht aus Deutschland. Rund 30 Professuren in aller Welt wurden mittlerweile mit ehemaligen Mitarbeitern Seebergers besetzt – ein globales Netzwerk der Wirkstoff- Forschung, das mindestens so verzweigt ist wie Kohlenhydratketten.
Der Wissenschaftler
Prof. Dr. Peter H. Seeberger
Peter H. Seeberger studierte Chemie in Erlangen und promovierte in Biochemie in Boulder, USA. Nach einem Forschungsaufenthalt am Sloan-Kettering Cancer Center in New York baute er am MIT in Cambridge eine eigene Arbeitsgruppe zur Kohlenhydrat-Synthese auf. Von der ETH Zürich wechselte er als Direktor ans Potsdamer Max-Planck-Institut für Kolloid- und Grenzflächenforschung und an die Freie Universität. Seine Forschungsergebnisse wurden international vielfach ausgezeichnet.
E-Mail: peter.seeberger@mpikg.mpg.de