Forschung an Alternativmethoden
„Tierversuche können nicht die Diversität des Menschen abbilden“
Professorin Monika Schäfer-Korting ist Initiatorin der Forschungsplattform BB3R
Bildquelle: Bernd Wannenmacher
Professorin Monika Schäfer-Korting, ehemalige Erste Vizepräsidentin der Freien Universität und Initiatorin der Forschungsplattform BB3R, ist eine der Vorreiterinnen auf dem Gebiet der Alternativmethoden zu Tierversuchen in Deutschland. Als Pharmakologin entwickelt sie mit ihrem Team bereits seit Anfang der 1990er-Jahre Hautmodelle auf Basis menschlicher Zellen. Catarina Pietschmann sprach mit ihr über Vorteile und Grenzen von tierversuchsfreien Testmethoden.
Kleine Nagetiere als Modell für Hauterkrankungen zu verwenden, ist bis heute ein Klassiker in der Pharmaforschung. Was brachte Sie dazu, auf menschliche Zellen umzusteigen?
Wenn es am Tier „geht“, sollte es auch am künstlichen Hautmodell funktionieren, war meine These. Außerdem leiden Menschen an diversen Erkrankungen, die bei Tieren gar nicht auftreten oder nur unzureichend induzierbar sind.
Anfangs wurden wir von vielen belächelt, aber bald gelang es uns genetische Hauterkrankungen wie das atopische Ekzem in vitro an Modellen aus Spenderhaut darzustellen. Später modellierten wir auch den hellen Hautkrebs und die sehr bösartigen Kopf-Hals-Karzinome. Aktuell arbeiten wir daran, nicht nur das Gewebe genau abzubilden, sondern auch die Therapie der jeweiligen Erkrankungen an den Modellen testen zu können, was im Fall des hellen Hautkrebses bereits funktioniert. Wir gewinnen die Hautzellen nicht nur aus Spenderhaut, sondern nutzen auch ausgezupfte Kopfhaare.
Die meisten Arzneimittel, darunter auch Hautsalben, wirken nicht nur örtlich (topisch), weil die Wirkstoffe über das Blut in den gesamten Organismus gelangen. Lassen sich systemische Wirkungen – und Nebenwirkungen – ebenfalls in künstlichen Modellen abbilden?
Ja, zum Beispiel an einem Multi-Organ-Chip. Diese Technologie wird von Professor Roland Lauster am Institut für Biotechnologie der TU Berlin entwickelt. Verbunden durch einen winzigen „Blutkreislauf“ überleben seine Miniaturorgane bis zu vier Wochen – deutlich länger als unsere Hautmodelle. Das ist ein ganz entscheidender Schritt für die Toxikologie. Denn bei der Prüfung von Chemikalien etwa ist ein 28-Tage-Test in der Risikoanalyse vorgesehen.
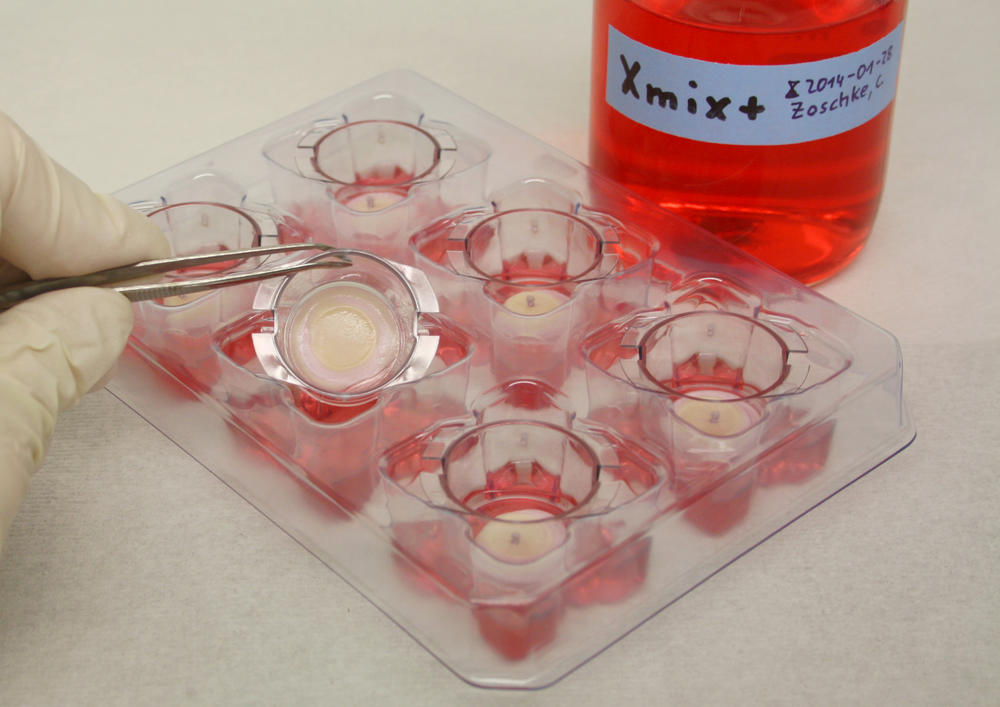
Aus Hautzellen züchten die Wissenschaftler Hautmodelle, an denen neue Anti-Krebswirkstoffe und andere Medikamente getestet werden können.
Bildquelle: Christian Zoschke
Was sind die Vorteile von Modellen aus Humanzellen?
Der Sprung von einer Spezies zur nächsten – zum Beispiel von Maus zu Mensch – ist extrem hoch. Insbesondere im Bereich der Haut. Inzwischen wissen wir, dass auch innerhalb unserer Spezies „Mensch“ eine enorme Diversität besteht. Es gibt deutliche Unterschiede in der Wirkung von Arzneimitteln auf Frauen und Männer, Kinder und Alte, Gesunde und Kranke, zudem können Begleiterkrankungen die Arzneimittelwirkungen beeinflussen.
Es wäre also wünschenswert, man könnte alle Faktoren, die im Einzelfall eine Rolle spielen (und letztlich Risiken bedeuten), im Voraus austesten. Aktuell geschieht das erst dann, wenn das Medikament einem gesunden Probanden oder dem Patienten verabreicht wird. An menschlichen Zellen lässt sich das im Vorfeld einfach besser erkennen als am Tier.
Bei Tierversuchen ist Diversität ja eher unerwünscht...
Aufgrund der 3 R werden Tierversuche standardisiert durchgeführt, um die im Versuch eingesetzte Tierzahl so gering wie möglich zu halten. Durch Gender in Medicine werden nun beide Geschlechter eingesetzt. Als ideales Versuchstier in der Arzneimittelforschung gilt immer noch die männliche Maus oder Ratte, steril aufgewachsen und genauso alt wie ihre „Mitprobanden“. Häufig sind die Tiere sogar aus dem selben Wurf.
Aus dem Contergan-Skandal in den 1960er-Jahren hat man allerdings Lehren für die Arzneimittelprüfung gezogen, wie beispielsweise die gesetzlich vorgeschriebene Embryotoxikologie im Rahmen der Zulassung von Medikamenten.
Kosmetika an Tieren zu testen ist in Deutschland seit 2013 verboten. Glauben Sie, dass man irgendwann auch in der Pharmaforschung vollständig darauf verzichten kann?
Definitiv nein. Nach Screening, Computersimulationen und in-vitro-Tests tausender Substanzen bleiben heute vergleichsweise nur noch wenige Kandidaten für ein neues Medikament übrig. Diese werden bislang umfassend auf Wirksamkeit und Sicherheit im Tiermodell getestet. Statistisch sind davon 8,6 Substanzen so erfolgreich, dass sie, im nächsten Schritt, in die klinische Prüfung kommen. Am Ende erweisen sich aber von diesen 8,6 umfassend untersuchten Arzneistoffkandidaten im Mittel nur 1,6 als für den Menschen geeignet! Vieles, was beim Tier optimal wirkt, versagt beim Menschen: 51 Prozent scheiden auf der Zielgeraden aus, weil sie unwirksam sind. 18 Prozent haben unerwartete Nebenwirkungen, die nicht tolerierbar sind. Der Mensch ist eben keine 70 Kilo schwere Ratte, wie ein Kollege aus Baltimore so schön sagte.
Der letzte Zwischenschritt – einen Arzneistoffkandidaten, der sich in Tests an rekonstruierten menschlichen Organen bewährt hat, am Tier zu testen bevor wir ihn erstmals am Menschen anwenden – ist gesetzlich für die Zulassung von Medikamenten vorgeschrieben. Aus humanethischen Gründen können wir darauf nicht verzichten.
Und wie sieht es in der biologischen Grundlagenforschung aus? In diesem Bereich finden über 40 Prozent aller Tierversuche in der EU statt.
Auch da wird es wahrscheinlich nie ganz ohne gehen. Biologen entdecken immer wieder einzigartige Eigenschaften an Lebewesen, die von großem Interesse für die Humanmedizin sind, und zu deren Entschlüsselung Tierversuche nötig sind.
Der unscheinbare Nacktmull zum Beispiel ist ein Säugetier wie wir – bekommt aber keinen Krebs! Was ist bei ihm anders als bei Maus und Mensch? Er lebt im Dunkeln, ist voller Runzeln und gänzlich haarlos – was aber ist für das fehlende Auftreten von Tumoren verantwortlich? Das lässt sich, zumindest bislang, in keinem Modell nachstellen. Ähnlich ist es bei der unglaublichen Regenerationsfähigkeit von Axolotln oder Plattwürmern.